Механизм самосборки коллагена оказался похож на застежку-молнию
В Байройтском университете в Германии раскрыли механизм, благодаря которому коллаген — самый распространенный белок в человеческом организме — успешно самоорганизуется. Выявлены электростатические силы, которые поддерживают эту самосборку и способствуют стабильности белка. Исследование вышло в журнале Nature Communications.
Зачем это нужно
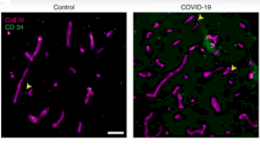
Коллагены — самые распространенные белки в человеческом теле, присутствующие в коже, костях, зубах и роговице. Генетически обусловленные нарушения их формирования приводят к тяжелым наследственным заболеваниям — например, несовершенному остеогенезу (хрупкости костей), при котором минимальное воздействие может стать причиной перелома.
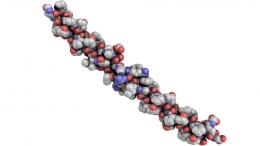
На молекулярном уровне коллаген представляет собой похожую на канат структуру из трех переплетенных нитей, известную как тройная спираль. Самоорганизация коллагена начинается с одного конца этой спирали и продвигается, как застежка-молния, к другому. Однако отдельные нити часто бывают слишком длинными и гибкими, что нарушает этот процесс.
Исследователи из рабочей группы «Коллаген — структура, функция и биоматериалы» под руководством доктора Абхишека Джалана с кафедры биоматериалов Байройтского университета идентифицировали электростатические молекулярные силы, которые стабилизируют уже сформированные участки тройной спирали, чем помогают самосборке оставшихся сегментов нитей.
Молекулярные зажимы
Секрет прочности коллагена — в правильном порядке аминокислот. Положительно заряженный лизин и отрицательно заряженный глутамат или аспартат образуют друг с другом мостики.
«Мостики между аминокислотами действуют как электростатические зажимы, фиксируя уже переплетенные нити тройной спирали и позволяя оставшимся участкам нитей организоваться. Эти мостики также предотвращают локальное распутывание уже сформированных участков коллагена», — объяснил Джалан.
В каждом из 28 известных типов коллагена в среднем содержится около 50 таких мостиков, причем вблизи нерегулярных участков их плотность выше. В «бракованном» коллагене таких мостиков намного меньше.
Мутации, которые с этим связаны, могут приводить к различным патологиям.
«Например, несовершенный остеогенез имеет широкий спектр тяжести. Какие-то формы не проявляются клинически, а другие приводят к летальному исходу. Влияние мутаций на солевые мостики впервые объясняет, почему существует такой спектр и почему некоторые мутации в коллагене вызывают более серьезные последствия, чем другие», — подытожил Джалан.
Схожая схема самосборки характерна для коллагеноподобных белков архей, бактерий, эукариот и вирусов, что указывает на универсальность этого механизма.